Semana 12 martes
CUANTIZACIÓN DE LA ENERGÍA
Planck postuló que la emisión de radiación electromagnética se produce en forma de "paquetes" o "cuantos" de energía(fotones). Esto significa que la radiación no es continua, es decir, los átomos no pueden absorber o emitir cualquier valor de energía, sino sólo unos valores concretos.
ESTRUCTURA DE LA MATERIA: ÁTOMOS Y MOLÉCULAS
La materia consiste de partículas extremadamente pequeñas agrupadas juntas para formar el átomo. Hay una 90 ocurrencias naturales de estas agrupaciones de partículas llamadas elementos.
Estos elementos fueron agrupados en la tabla periódica de los elementos en secuencia de acuerdo a sus números atómicos y peso atómico. Hay además 23 elementos hechos por el hombre que no ocurren en la naturaleza, por lo que al final son unos 113 elementos conocidos hasta la fecha. Estos elementos no pueden cambiarse por procesos químicos. Ellos solo pueden ser cambiados por reacción nuclear o atómica, sin embargo pueden ser combinados para producir el incontable número de compuestos con los que tropezamos día a día.
ESTRUCTURA DEL ÁTOMO
Un átomo puede ser representado simbólicamente en un modelo que recrea nuestro sistema solar, el cual tiene en el centro el sol y los planetas girando en órbitas alrededor de él.
Este modelo atómico, representado en la figura 1 fue propuesto por el físico Danés, Niels Bohr en 1913. Los mecanismos cuánticos actuales han demostrado que este modelo no es exactamente correcto, pero sigue siendo útil para la visualización de átomo.
El centro del átomo se llama núcleo y está principalmente formado por las partículas llamadas Protones y Neutrones, los que constituyen la mayoría de la masa del átomo. Orbitando alrededor del los núcleos están pequeñas partículas llamadas electrones. Estos electrones tienen una masa muchas veces mas pequeña que el Protón y el Neutrón. Hay otras partículas sub-atómicas estudiadas por los físicos atómicos, pero estas tres son suficientes para nuestro propósito.
ESTRUCTURA DE LAS MOLÉCULAS
La geometría molecular o estructura molecular se refiere a la disposición tridimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, reactividad, polaridad, fase, color, magnetismo, actividad biológica, etc. Actualmente, el principal modelo es la teoría de repulsión de pares de electrones de valencia (TRPEV), empleada internacionalmente por su gran predictibilidad.
ESPECTROS DE EMISIÓN/ABSORCIÓN DE GASES
ESPECTROS DE EMISIÓN
El espectro de emisión atómica de un elemento es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento, en estado gaseoso, cuando se le comunica energía. El espectro de emisión de cada elemento es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
La frecuencia es igual a:
Planck postuló que la emisión de radiación electromagnética se produce en forma de "paquetes" o "cuantos" de energía(fotones). Esto significa que la radiación no es continua, es decir, los átomos no pueden absorber o emitir cualquier valor de energía, sino sólo unos valores concretos.
ESTRUCTURA DE LA MATERIA: ÁTOMOS Y MOLÉCULAS
La materia consiste de partículas extremadamente pequeñas agrupadas juntas para formar el átomo. Hay una 90 ocurrencias naturales de estas agrupaciones de partículas llamadas elementos.
Estos elementos fueron agrupados en la tabla periódica de los elementos en secuencia de acuerdo a sus números atómicos y peso atómico. Hay además 23 elementos hechos por el hombre que no ocurren en la naturaleza, por lo que al final son unos 113 elementos conocidos hasta la fecha. Estos elementos no pueden cambiarse por procesos químicos. Ellos solo pueden ser cambiados por reacción nuclear o atómica, sin embargo pueden ser combinados para producir el incontable número de compuestos con los que tropezamos día a día.
ESTRUCTURA DEL ÁTOMO
Un átomo puede ser representado simbólicamente en un modelo que recrea nuestro sistema solar, el cual tiene en el centro el sol y los planetas girando en órbitas alrededor de él.
Este modelo atómico, representado en la figura 1 fue propuesto por el físico Danés, Niels Bohr en 1913. Los mecanismos cuánticos actuales han demostrado que este modelo no es exactamente correcto, pero sigue siendo útil para la visualización de átomo.
El centro del átomo se llama núcleo y está principalmente formado por las partículas llamadas Protones y Neutrones, los que constituyen la mayoría de la masa del átomo. Orbitando alrededor del los núcleos están pequeñas partículas llamadas electrones. Estos electrones tienen una masa muchas veces mas pequeña que el Protón y el Neutrón. Hay otras partículas sub-atómicas estudiadas por los físicos atómicos, pero estas tres son suficientes para nuestro propósito.
ESTRUCTURA DE LAS MOLÉCULAS
La geometría molecular o estructura molecular se refiere a la disposición tridimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, reactividad, polaridad, fase, color, magnetismo, actividad biológica, etc. Actualmente, el principal modelo es la teoría de repulsión de pares de electrones de valencia (TRPEV), empleada internacionalmente por su gran predictibilidad.
ESPECTROS DE EMISIÓN/ABSORCIÓN DE GASES
ESPECTROS DE EMISIÓN
El espectro de emisión atómica de un elemento es un conjunto de frecuencias de las ondas electromagnéticas emitidas por átomos de ese elemento, en estado gaseoso, cuando se le comunica energía. El espectro de emisión de cada elemento es único y puede ser usado para determinar si ese elemento es parte de un compuesto desconocido.
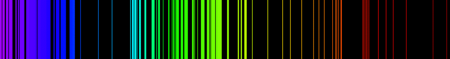
Las características del espectro de emisión en algunos elementos son claramente visibles cuando estos elementos son calentados. Por ejemplo, cuando un alambre de platino es bañado en una solución de nitrato de estroncio y después es introducido en una llama, los átomos de estroncio emiten color rojo. De manera similar, cuando el Cobre es introducido en una llama, ésta emitirá una luz verde. Estas caracterizaciones permiten identificar los elementos mediante su espectro de emisión atómica.
El hecho de que sólo algunos colores aparezcan en las emisiones atómicas de los elementos significa que sólo determinadas frecuencias de luz son emitidas. Cada una de estas frecuencias están relacionadas con la energía de la fórmula:
donde :
- es la energía del fotón
- es la constante de Planck
- es la frecuencia
La frecuencia es igual a:
donde:
- es la velocidad de la luz en el vacío
- es la longitud de onda
Con esto se concluye que sólo algunos fotones con ciertas energías son emitidos por el átomo. El principio del espectro de emisión atómica explica la variedad de colores en signos de neón, así como los resultados de las pruebas de las llamas químicas mencionadas anteriormente.
Las frecuencias de luz que un átomo puede emitir depende de los estados en que los electrones pueden estar. Cuando están excitados, los electrones se mueven hacia una capa de energía superior. Y cuando caen hacia su órbita normal emiten la luz.
ABSORCIÓN DE GASES
La absorción de gases es una operación unitaria en la cual una mezcla gaseosa se pone en contacto con un líquido, a fin de disolver de manera selectiva uno o más componentes del gas y de obtener una solución de éstos en el líquido.
SEMANA12
SESIÓN
34
|
Física 2
1.Cuantización de la materia y la energía
|
contenido temático
|
• Cuantización de la energía
• Estructura de la materia: átomos y moléculas.
|
Aprendizajes esperados del grupo
|
Conceptuales
• Reconoce los modelos elementales de la estructura de la materia. N1.
• Describe algunos espectros de gases y su relación con la estructura de los átomos. N1.
Procedimentales
· Elaboración de modelos en transparencias Power Point (.pps) y manejo del proyector.
· Presentación en equipo
Actitudinales
| |||||||||||||||||||||||
Materiales generales
|
Computo:
- PC, Conexión a internet
De proyección:
- Cañón Proyector
Programas:
- Moodle, Google docs, correo electronico, Excel, Word, Power Point.
Didáctico:
- Video el “Átomo de Bohr.”
| |||||||||||||||||||||||
Desarrollo del proceso
|
FASE DE APERTURA
- El Profesor hace la presentación de la pregunta:
Al asumir que la energía sólo puede ser absorbida o liberada en paquetes discretos, pequeños, diferenciales, que llamó "paquetes" o "elementos de energía"
Planck explicó el hecho de que ciertos objetos cambiaban de color cuando se calentaban
Investigación sobre el fenómeno de la radiactividad y actividad de simulación con dados/monedas.
• Observación de los espectros de emisión de algunos gases usando lámparas de descarga y un disco compacto como rejilla de difracción y descripción de ellos.
- Los alumnos en equipo, discuten y escriben sus respuestas en el cuadro, utilizando el procesador de palabras:
FASE DE DESARROLLO
El Profesor presenta a los alumnos el video “El átomo de Bohr”, los alumnos
Elaboran un resumen de acuerdo a las indicaciones del Profesor.
- El Profesor solicita a los alumnos que se numeren en forma consecutiva, y de acuerdo a su número dibujen el modelo atómico del elemento de acuerdo al modelo atómico de Bohr. Lo presenten en diapositiva Power Point.
- Los alumnos discuten y obtiene conclusiones.
FASE DE CIERRE
Al final de las presentaciones, se lleva a cabo una discusión extensa, en la clase, de lo que se aprendió y aclaración de dudas por parte del Profesor.
Actividad Extra clase:
Los alumnos llevaran la información a su casa y los que tengan computadora e internet, indagaran los temas de la siguiente sesión, de acuerdo al cronograma.
Los alumnos que tengan PC y Programas elaboraran su informe, empleando el programa Word, para registrar los resultados.
| |||||||||||||||||||||||
Evaluación
|
Informe en Power Point de la actividad.
Contenido:
Resumen de la Actividad.
|








Comentarios
Publicar un comentario